Yamaton Kプロジェクト
新たに人腎臓を作りだすプロジェクトをYamaton Kと称して、15年の歳月をかけて進めてきた。
ここで言うYamatoとは日本の古い名称・大和である。そしてtonとは、日本語でブタの意味である。
KとはKidneyの頭文字である。同様に肝臓を作り上げるプロジェクトはLiverの頭文字を取り、Yamaton Lプロジェクトと名付けられている。
胎児の臓器が出来上がる仕組みを理解して
それを利用するコンセプトの展開
動物の胎仔に人の幹細胞を打ち込むと、異種免疫反応を乗り越えキメラ臓器ができる現象がある。すなわち免疫機能ができていないうちにヒト幹細胞等を異種動物の胎仔に打ちこみ、動物胎仔の発育過程を利用してヒト幹細胞の臓器への分化を誘導する手法である。
古くはMackenzieらが、ヒトMSCを羊の胎仔に経子宮的に注入して分化誘導かけた報告がある(Mackenzie 2001)。この動物胎仔へのヒトMSC注入し腎臓のオルガノイドを作製させる手法は、横尾らの人工子宮装置実験で直接証明された(Yokoo T, 2005)。さらに中内らによる胚盤胞置換術により異種動物の受精卵へiPS/ES細胞を打ちこむことと異種動物側の腎臓発生に関わる遺伝子(この場合はSall 1)をノックアウトすることで打ちこまれる幹細胞側の遺伝子が補完し、臓器発生するする研究がなされている(Usui 2012)。これらはヒトの細胞が動物の体を借りて増殖・分化し、臓器として成熟するという動物工場(In Vivo Bioreactor)という考え方に基づく。
一方、出来上がりつつある臓器の芽を患者に移植し、患者自身の体内で育て上げる治療法がある。Organ But Transplantation(臓器の芽の移植)という、ヒト臓器の芽を試験管で作り上げ、これを患者に移植して患者体内で育て上げようとする手法である。
試験管レベルでは長船らは、マウスの胎仔腎臓細胞とヒトiPS細胞から誘導した中間中胚葉細胞の共培養からヒト遠位尿管を作り上げた(Mae, 2013)。また西中村らはヒトiPS細胞から体軸幹細胞、さらに腎臓前駆細胞作り、この細胞とマウスの胎仔脊髄を接触培養することでヒト糸球体と尿細管を作った(Sakaguchi, 2013)。いずれの仕事も腎臓発生のメカニズムを明らかにし、3次元の腎臓の構造を作り上げる一歩である。この臓器の芽を異種動物の胎仔の臓器に注目した仕事として、古くはHammermanらがブタ胎仔を用いて腎臓や膵臓の臓器の芽を使って行なってきている(Takeda S, 2006)。
横尾は、ラット胎仔腎臓を取り出し、体外でヒトMSCを注入して、再度成熟したラット体内に戻し、ヒトの幹細胞が腎臓の細胞に分化することを証明した(Yokoo T, 2006, 2008)。Yamaton Kプロジェクトは、この基礎的実験史実をもとに、ヒトへの応用を目指し、大型動物への挑戦として始まった。
前臨床としての大型動物実験への挑戦
ブタの腎臓原基をネコに移植する実験に着手した。ヒト患者への応用は、従来の異種移植と同等の手続が必要であり、安全性確立に大きなハードルがあるために、むしろペット猫での有効性と安全性の検証することを第一次的目標として北里大学獣医学部・岩井聡美と明治大学農学部・長嶋比呂志らと共同研究を進めた。

2008年チームYamaton K
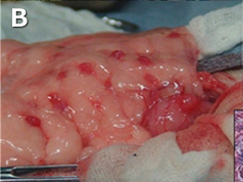
手術を受けた猫の体網内で
発育する腎臓原基
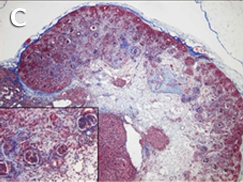
移植1カ月後の移植腎臓原基
小林は大塚製薬工場の特別顧問となり、企業予算を投じ、人の体サイズを概想して、ブタ-ブタ間での検証を進めた。免疫制御により腎臓原基は育つことが判明し、尿管を伸ばす移植腎臓原基を得ることができた。

2010年チームYamaton K
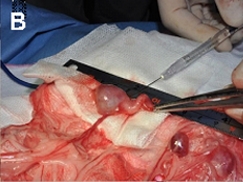
ブタ-ブタ間での移植で発育し尿を
蓄積した腎
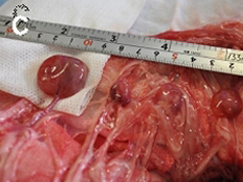
ブタ-ブタ間での移植で発育し尿を
蓄積した腎
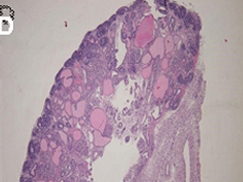
尿の蓄積により水腎症化した
移植腎臓原基
一方、動物の腎臓の芽にヒトの体幹細胞であるMSCを中に入れてヒトキメラ化を強める手法の研究が進められた。このヒトのMSCを持ったブタの腎臓の芽が患者体内で発育を起こさせるためには免疫抑制薬が一時的に必要であるが、ある程度ヒト幹細胞が腎臓の細胞に分化誘導がかかった段階でブタ組織が薬剤で消滅できれば、完全なヒト化組織が出来上がる可能性を小動物モデルで示した(Matsumoto, 2012)。
それまでの腎臓原基グラフトを膀胱・尿路と一塊にして採取するクロアカグラフトを開発した。それまでの片側の腎臓の芽(メタネフロン)では、腎臓が発育し始め産生される尿を一時的にレザーブできる組織をどのように作るかが大きな課題であった。そして、その尿を本来の尿管と接合して、体外に誘導するルートを作る画期的な外科的な技術であった。

2012-3年チームYamaton K
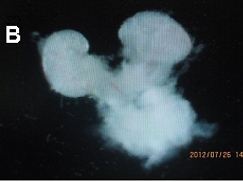
新開発された豚クロアカグラフト
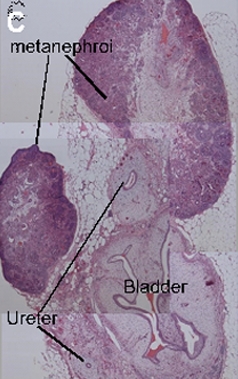
猫に移植され発育した
豚クロアカグラフト
小林は慶應大学医学部に移転し、臓器再生医学寄付講座を開設した。そして非臨床・臨床一体型研究開発手法を展開するため学閥を乗り越えたピッグコンソーシアムを作り始めた。
開発したクロアカグラフトは、腎不全動物の体内でも育ち、新たに産生された尿はクロアカグラフトの膀胱に貯留し、レシピエントの尿管と吻合できる技術となった(Yokote. 2015)。
さらに横尾らは、ヒトiPS細胞由来細胞を異種の腎臓原器移植し、ヒト由来細胞が腎臓へと分化した段階で異種動物の組織を選択的に消去する手法をさらに現実化するため小動物モデルを展開した(Yamanaka S, 2017)。

2014年定期ミーテングでのYamatonKチーム
ブタクロアカにヒトiPS由来腎前駆細胞を体外で打ち込み、それを他のブタに移植するという臨床を想定したプロトコールの検証が始まった。
2018年富士マイクラ社実験室でブタ実験をする慈恵メンバー
この腎再生プロジェクトは、AMED研究に採択され、大日本住友製薬との共同研究により、サルをレシピエントとした最終プロトコールでの検証へと進んだ。
大日本住友製薬株式会社
腎臓の再生医療実現に向けた …
大日本住友製薬株式会社へ
2019年大日本住友製薬実験室での慈恵YamatonKチーム
